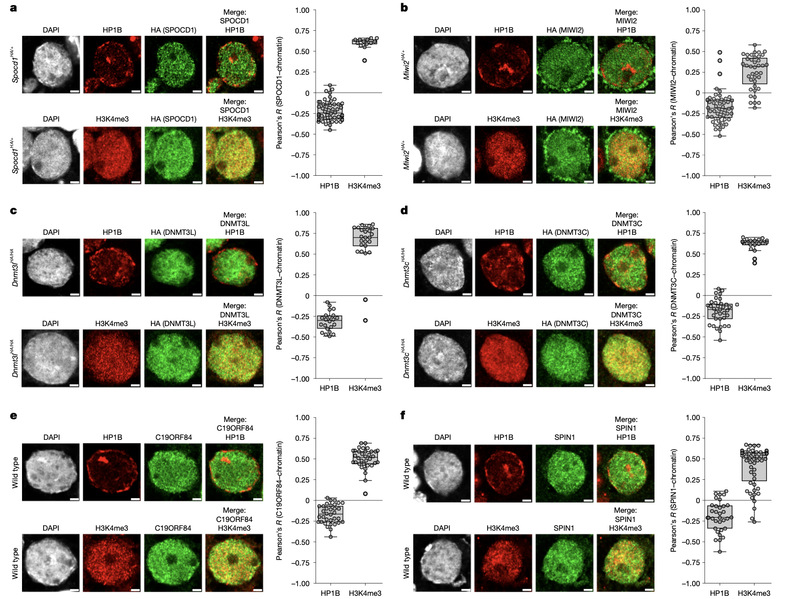
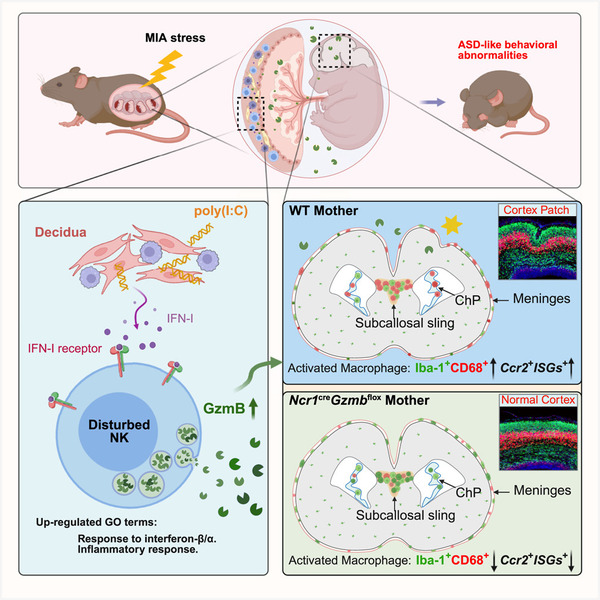
PGT(Preimplantation Genetic Testing)即胚胎植入前遗传学检测,又称为“第三代试管婴儿”,是指在辅助生殖过程中对植入前的胚胎进行基因突变或染色体检测, 选择正常的胚胎植入宫腔, 以降低家族遗传性疾病,染色体异常及反复流产等风险的遗传学检测技术。传统意义上的PGT主要包含三类:1、减少流产及植入失败的风险的胚胎植入前染色体非整倍体检测(PGT-A, PGT for Aneuploidies);2、适用于平衡易位或其他结构重排的患者,减少流产的风险和预防与不平衡染色体组型导致的染色体疾病的胚胎植入前染色体结构异常检测(PGT-SR, PGT for Chromosomal Structural Rearrangement);3、适用于单基因疾病患者,防止子代遗传疾病的发生的胚胎植入前单基因遗传病检测(PGT-M, PGT for Monogenic/Signle gene)。
多基因遗传病是由微效多基因与环境共同作用导致的,如慢性疾病冠心病、糖尿病、肿瘤、肥胖、精神分裂症、高血压、唇腭裂等。这些疾病通常有较高的遗传度,具有家族聚集倾向,患者一级亲属的发病率高于群体发病率,且患者的亲缘关系越近,发病风险越高,提示遗传基础在决定个体的患病风险上起了较为重要的作用。
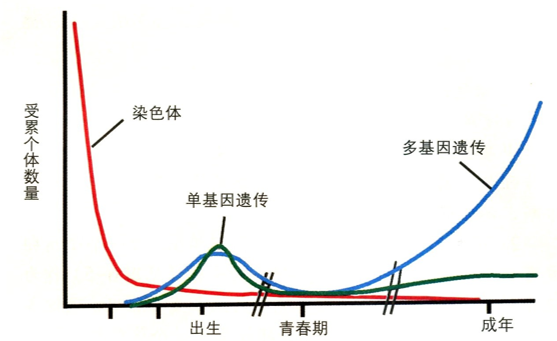
相较于可明确针对由遗传因素导致的染色体病或单基因遗传病等疾病进行阻断、却受限于多基因疾病的传统三代试管(PGT)检测,PGT-P(PGT for polygenic disorders)作为一种新的优生优育技术,对包含2型糖尿病、冠心病等在内的复杂疾病,通过多基因遗传风险评分方法对胚胎进行多基因疾病遗传风险评估,筛选疾病风险最低的胚胎移植,从而实现多基因遗传病的一级防控。该技术在源头上对重大的慢病进行控制,进而降低多基因遗传病的风险,其主要目的是降低人群多基因疾病发生率,是慢病防控关口前移的一个重要举措。
2型糖尿病也属于多基因遗传病。目前国人2型糖尿病参考基因组数据库缺乏,无法通过常规的PGT进行阻断。通过黄荷凤院士团队的潜心研究,将基于大规模GWAS数据建立的2型糖尿病全基因组检测和多基因风险评分(polygenic risk score,PRS)模型,先在英国生物标本库(UK Biobank)的50多万名对照人群、27497个2型糖尿病个体中进行风险评分算法的测试和验证,再根据家庭遗传背景和性别等因素对不同的风险位点分配不同的权重,构建基于个性化家庭的PRS+模型,以克服常规建立的PRS模型在欧洲人群中预测较为准确,而在非欧洲队列中准确性有限的短板。2022年,在黄荷凤院士的带领下,团队通过基于chromSwift扩增技术和基因型填充的策略,对胚胎进行遗传风险评估,成功筛选疾病风险最低的胚胎移植。由此,不仅是中国首例,更是全球首个基于家系遗传信息的PGT-P技术优选出来的2型糖尿病低风险试管婴儿在复旦大学附属妇产科医院顺利诞生。复旦大学附属妇产科医院作为PGT-P技术的先行者,在中国迈出了多基因遗传病源头防控的第一步。

目前高血压、糖尿病等复杂疾病流行趋势日益增加,但预防效果不理想,长期以来患者的健康管理和治疗往往带来沉重负担。黄荷凤院士团队另辟蹊径,从新角度寻求突破:建立属于中国人群的基因数据库,通过与基因库对照,提前预警、诊断个人慢性病的发病风险,同时,通过多基因分析和评分,还可以优化个人的治疗策略,使用对基因最敏感的药物进行治疗。此举在辅助生殖发展历程中具有重要意义,同时也为未来其他与遗传高度相关的慢性疾病的源头防控提供了理论与技术依据。今后,团队还将对乳腺癌等多基因病开展PGT-P的防控。


 EN
EN